【ZiDongHua 之创新自科文收录关键词: 清华大学 自动化系 显微镜 人工智能】
紫冬学术 | 戴琼海/吴嘉敏/俞立团队发布共聚焦扫描光场显微镜:活体长时程高速三维高分辨观测新利器
越来越多的研究发现体外与活体环境间的巨大差异会显著影响细胞的功能与表型。大量生理与病理状态下不同类型细胞间的交互作用难以在体外复现。因此,在哺乳动物活体原位对细胞及亚细胞的高速变化进行长时程观测变得尤为重要。然而,目前常用的活体显微成像技术如转盘共焦显微镜(spinning disk confocal microscope,SDCM)和双光子显微镜(two-photon microscopy),虽然通过共聚焦探测和非线性激发的方式有效去除了背景荧光干扰,但仍然面临三维成像速度慢,光毒性大,组织像差引起的分辨率低等重要问题,难以满足日益增长的活体观测需求。清华大学团队于2021年提出扫描光场显微镜(scanning light-field microscopy, sLFM)(详见BioArt报道:Cell突破|戴琼海团队以前所未有的时空分辨率进行哺乳动物活体长时程观测)【1】,能够以相机帧率的超高速实现三维高分辨率观测,并将光毒性降低了三个数量级,为活体多细胞间交互研究打开了大门,但在一些复杂组织和样本中仍然面临强背景荧光干扰,相比于共聚焦探测损失了成像对比度。
针对这一难题,2024年5月27日,Nature Biotechnology杂志在线发表了清华大学戴琼海、吴嘉敏、俞立与浙江荷湖科技有限公司合作完成的题为Long-term intravital subcellular imaging with confocal scanning light-field microscopy的研究论文【2】。团队历经三年多的技术攻关和落地转化,在扫描光场显微镜的基础上引入了线扫描共聚焦模块,配合全新的三维重建算法,研制了新一代的共聚焦扫描光场显微镜(csLFM),兼具两者的性能优势。csLFM拥有跟共聚焦显微镜一致的光学层析能力,即使在深层组织或密集标记的荧光样本中依然能保持高对比度,同时三维成像速度相比转盘共聚焦显微镜SDCM提高了100倍,光毒性降低了130倍,打破了并行度与保真度间的矛盾。csLFM将替代传统共聚焦显微镜,为科学家在活体复杂环境中获得更真实、可靠的细胞及亚细胞结构间相互作用信息提供前所未有的研究工具,支撑脑科学、免疫学、病理学等基础学科产生重大突破。

团队前期开发的扫描光场显微镜已经在高速亚细胞分辨率长时程三维观测上具备显著优势,如何兼具光学层析能力是进一步提高其在多样性生命科学与医学应用中保持稳定鲁棒的成像质量和实用性的关键所在。如图1所示,共聚焦扫描光场显微镜csLFM巧妙地通过轴向拓展的线扫照明与相机本身的滚动快门将共聚焦策略整合到扫描光场显微镜sLFM中。由于扫描光场显微镜天然的三维感知能力,无需非常小的狭缝或者小孔去除背景荧光,轴向拓展的线扫照明能够在不损失三维光效率和三维成像速度的前提下对有效三维成像范围外的背景荧光进行特异性的去除,将图像的信背比 (signal-to-background ratio, SBR) 提升了12 dB,具备与共聚焦显微镜一致的光学层析能力,并在数字自适应光学的支撑下在复杂环境中保持了近衍射极限的三维高分辨率,精确捕捉细胞器等亚细胞结构。
脾脏在免疫功能方面扮演着重要角色,其含有大量的免疫细胞和多种免疫分子。但因组织密集、强背景荧光以及对光损伤的敏感性,脾脏中细胞和亚细胞水平的成像极具挑战性。研究人员凭借csLFM出色的光学层析性能和极低的光毒性,在国际上首次实现了脾脏内免疫微环境连续数小时的毫秒级高速三维高分辨率观测,并精细刻画了免疫系统在自然状态下如何协同工作。研究人员意外地观察到NK细胞通过收缩丝体与巨噬细胞粘附,并在巨噬细胞内定向产生迁移体,该迁移体传递现象也是首次在除了中性粒细胞之外的其他免疫细胞中观察到,提示迁移体传递可能是一种增强先天适应性免疫监视的信号协同机制。更进一步地,csLFM作为一个通用的活体成像框架,在有效去除背景荧光及其带来的光子噪声后,能够精细地分辨微小的细胞器结构。例如,尺寸仅为50-250nm的收缩丝体,其在小鼠体内的生成过程清晰地被csLFM动态呈现。
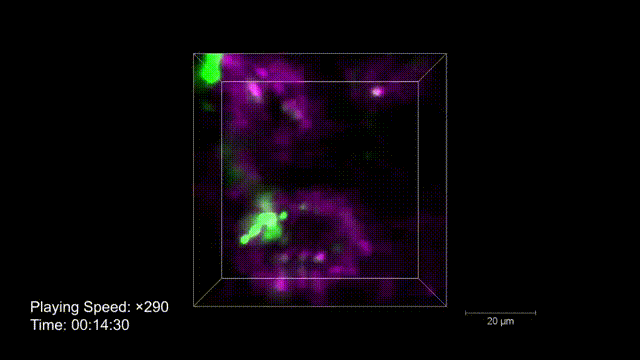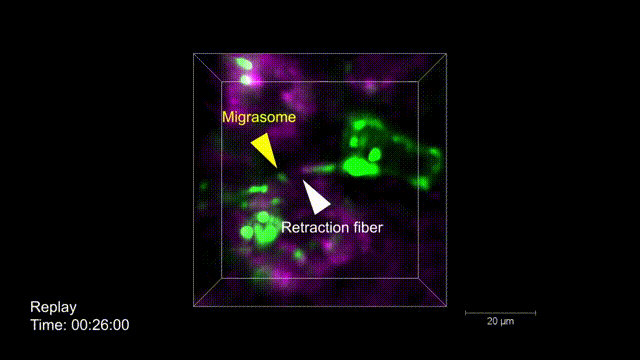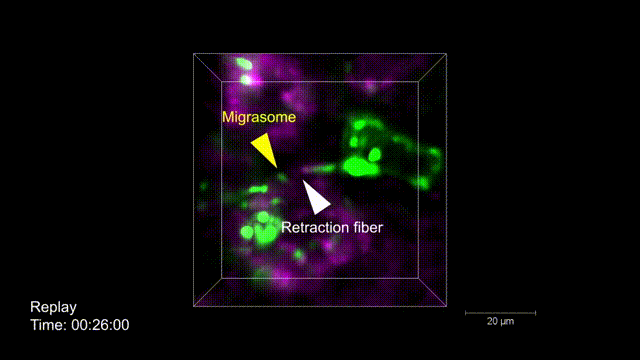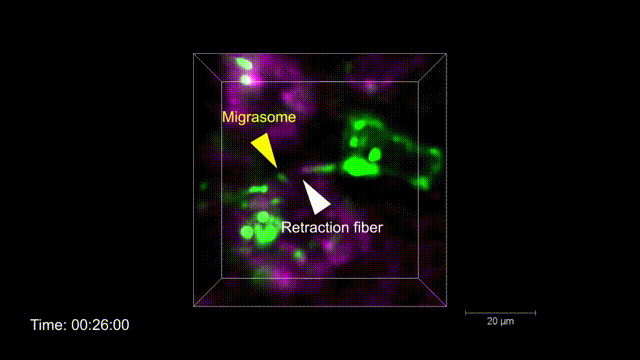
图2 | 活体小鼠脾脏体内迁移体传递过程的高速高分辨高保真三维成像
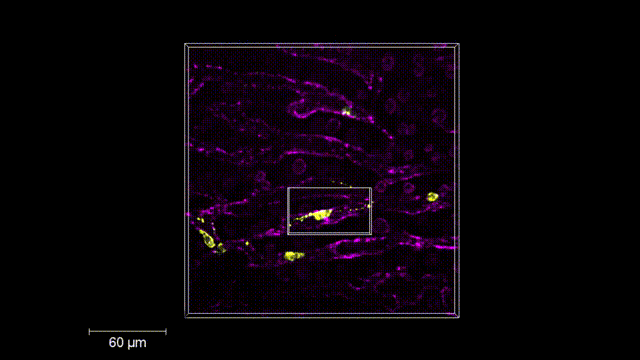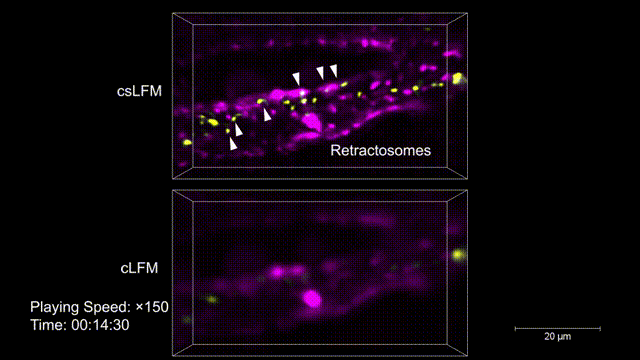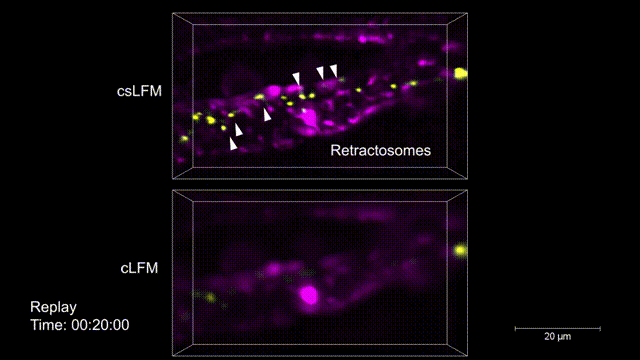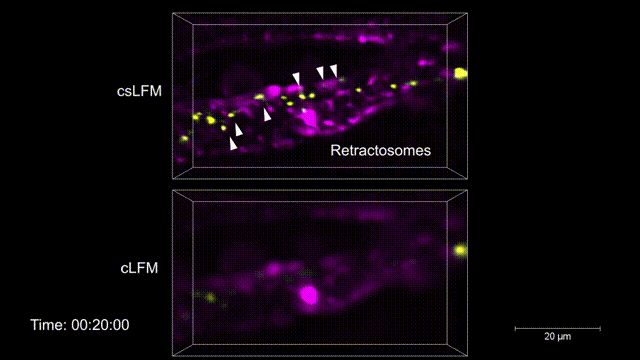
图3 | 活体小鼠体内收缩丝体(50-250nm)的三维快速生成过程监控
方向选择性在视觉神经编码过程中起关键作用。研究人员利用csLFM记录了动态光栅刺激下小鼠初级视觉皮层多个神经元的钙活动,来评估对视觉刺激有反应的神经元的调谐特性。尽管扫描光场显微镜相比于传统宽场显微镜已经显著去除了背景信号的干扰,但仍然有一些弱信号被淹没于巨大的背景信号中,特别在密集神经元标记的状态下,共聚焦扫描光场显微镜极大地削弱了大脑组织散射和密集荧光标记带来的背景串扰。定量结果表明,csLFM在皮层200-300微米的深度中,获得的神经元方向选择性指数(OSI)达52%,与双光子显微镜的成像性能相媲美并具备更高的空间分辨率。csLFM有望广泛应用于脑科学研究中,研究神经元与不同类型细胞间的动态交互过程。
跨膜电压指示剂可以对单个神经元内毫秒级响应进行检测,为在体大范围电生理记录提供了可能。然而,该技术也对显微成像技术也提出了巨大的挑战。csLFM在国际上首次实现对一个清醒的果蝇大脑中几乎所有的多巴胺能神经元进行大规模高保真信号记录,成像深度达100微米,速度高达为150帧/秒。对比数据表明,csLFM识别的神经尖峰数量比sLFM增加了近3倍和脉冲幅度增强了1.5倍。此外,csLFM还可以将sLFM中被背景淹没的弱电压信号高保真地识别出来。该方法有力推进了电压指示剂在神经科学中的应用,助力对神经环路功能和机制的精细化认识,对由神经环路发育异常引起的相关疾病诊断和治疗有重大意义。
据悉,该突破性技术已落地转化为显微仪器产品SLiM2000。这也是研究团队产学研同步推进的首次尝试,在原理技术发表的同时推出量产的商业化系统。为了弥合学术研究原理样机与商用仪器之间的鸿沟,满足基础研究对先进仪器的迫切需求,过去三年多的时间里,SLiM2000理论技术研究与工程化产品研发双管齐下。SLiM2000仪器产品已于近日与学术论文同时正式发布(http://www.hehutek.com/cn/product/slim2000)。该产品在分辨率和光学层析性能与转盘共聚焦显微镜保持一致的情况下,支持高达每秒150帧的亚细胞分辨率高保真三维成像,三维成像速度提升100倍以上。同时还配置有自动化的电动位移台,搭配定制化的样品适配器,实现实时自动聚焦、自动追焦、实时渲染,借助人工智能分析,以获取更快的结果跟踪和更为深入的数据分析,并能直接与团队前期开发的去噪软件等兼容。助力高速神经成像、免疫微环境观测等大规模活体细胞间相互作用的研究。
清华大学自动化系博士后卢志、博士生左思清、生命学院博士生史明慧为该论文的共同第一作者,清华大学自动化系、北京信息科学与技术国家研究中心、脑与认知科学研究院、清华-IDG/麦戈文脑科学研究院戴琼海教授,吴嘉敏副教授,生命学院俞立教授为论文共同通讯作者。
原文链接:点击文末“阅读原文”
参考文献
1. Wu, J. et al. Iterative tomography with digital adaptive optics permits hour-long intravital observation of 3D subcellular dynamics at millisecond scale. Cell 184, 3318-3332 (2021).
2. Lu, Z. et al. Long-term intravital subcellular imaging with confocal scanning light-field microscopy. Nature Biotechnology (2024). https://doi.org/10.1038/s41587-024-02249-5





评论排行